    |
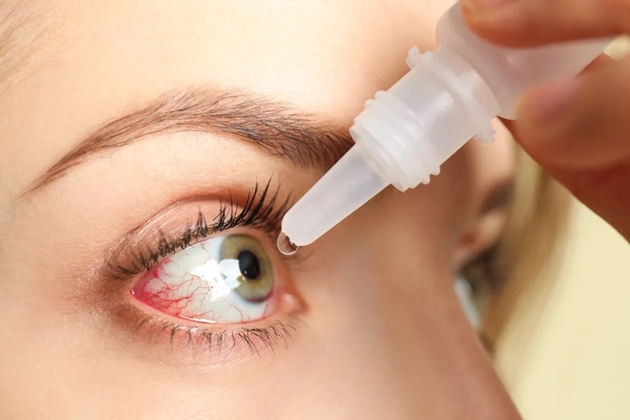 |
| Mỹ đã thu hồi một số thuốc nhỏ mắt sau khi phát hiện trường hợp tử vong, mù lòa. Ảnh:Shutterstock. |
Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh (CDC) Mỹ đã xác định được 68 bệnh nhân trên 16 tiểu bang mắc một chủng vi khuẩn Pseudomonas aeruginosa hiếm gặp, BBC đưa tin ngày 17/3.
Chủng này chưa bao giờ được tìm thấy ở Mỹ trước đợt bùng phát mới nhất này.
Ngoài một trường hợp tử vong, còn có 8 bệnh nhân bị giảm thị lực và 4 người phải phẫu thuật cắt bỏ nhãn cầu.
Theo CDC, hầu hết bệnh nhân được chẩn đoán nhiễm trùng đều sử dụng thuốc nhỏ mắt và nước mắt nhân tạo.
CDC cho biết ban đầu có 10 nhãn hiệu khác nhau được xác định là có thể liên quan đến vụ việc. Một số thuốc nhỏ mắt được sản xuất tại Ấn Độ và nhập khẩu vào Mỹ dưới hai nhãn hiệu sau đó đã bị rút khỏi thị trường vào tháng 1 và tháng 2.
Cụ thể, vào tháng 1, CDC đã cảnh báo mọi người ngừng sử dụng sản phẩm nước mắt nhân tạo EzriCare và Delsam Pharma.
Tháng tiếp theo, Global Pharma - công ty Ấn Độ có các sản phẩm mà hãng dược phẩm EzriCare và Delsam Pharma phân phối - đã ban hành lệnh thu hồi tự nguyện theo khuyến nghị chính thức từ Cơ quan Quản lý Thực phẩm và Dược phẩm Mỹ (FDA).
CDC cho biết qua xét nghiệm, các chai đã mở lấy từ bệnh nhân được phát hiện có chứa vi khuẩn. Các chai chưa mở hiện được xét nghiệm để xác định xem có nhiễm bẩn trong quá trình sản xuất hay không.
Tuần trước, một phụ nữ ở Florida đã kiện công ty dược phẩm, cho rằng cô bị nhiễm trùng sau khi sử dụng sản phẩm và các bác sĩ buộc phải cắt bỏ một bên mắt của cô.
Luật sư của người phụ nữ này đổ lỗi sự nhiễm khuẩn là do thiếu chất bảo quản trong thuốc nhỏ mắt.
“Có khả năng còn nhiều người bị nhiễm bệnh mà không hề hay biết”, luật sư Natasha Cortes nói với NBC News.
Một đại diện của EzriCare nói rằng các xét nghiệm cho đến nay vẫn chưa cho thấy mối liên hệ chắc chắn của đợt bùng phát với sản phẩm.
“Ở mức độ lớn nhất có thể, chúng tôi đã liên hệ với khách hàng để khuyên họ không nên tiếp tục sử dụng sản phẩm”, người phát ngôn của công ty cho biết. "Chúng tôi cũng ngay lập tức liên hệ với cả CDC và FDA, bày tỏ sự sẵn sàng hợp tác với bất kỳ yêu cầu nào họ đưa ra cho chúng tôi".
CDC cho biết bất kỳ ai đã sử dụng các sản phẩm bị thu hồi và đang có các triệu chứng nên liên hệ với bác sĩ.
Các triệu chứng bao gồm chảy dịch vàng, xanh lá cây, khó chịu hoặc đau, đỏ, mờ mắt và nhạy cảm với ánh sáng.
Tuần trước, FDA đã thông báo thu hồi riêng đối với một số sản phẩm thuốc nhỏ mắt do Pharmedica và Apotex phân phối.
Theo Statista, một công ty nghiên cứu thị trường, các sản phẩm nhỏ mắt và rửa mắt được khoảng 117 triệu người Mỹ sử dụng vào năm 2020.
Theo zingnews